快訊
- 快訊/美國最高法院判決川普關稅違法 「法律未授權總統徵收關稅」
- 日外相國會演說再提「竹島主權」 南韓召見公使抗議
- 美國去年第4季經濟成長放緩 全年成長為近3年最差
- 廉航德威加入 南韓所有航空禁止機上使用行動電源
- 日本最年輕冬奧金牌選手背後的男人:為她做飯、開車接送「妹妹總有一天會站上世界舞台」
- 江蕙唱一半見她衝上台突認有壓力 江淑娜搶穿戰袍討紅包
- 國道初四73起事故「回堵最長7公里」 明天北返車多!11條魔王路段曝光
- 前線照片打臉政府「沒埋地雷」說法 2柬埔寨記者遭叛國罪重判14年
- 江蕙大年初四重返小巨蛋 豪撒300個紅包
- 駐韓美軍黃海上空訓練、中國出動戰機 雙方一度對峙
- 訴訟纏身壓力大?英國快時尚ASOS創辦人泰國巴達雅墜樓亡
- 【更新】黃國昌二林拜票被嗆「臭俗辣」 嗆聲者遭志工拿糖塞嘴、候選人道歉
- 紫南宮前逃漏稅?手搖飲店公告「春節15天停開發票」挨罵 總部道歉
- 天乾物燥 日本下關寺廟失火、一家5口俱亡
- 33年來首見!美自台進口金額超越中國 汪浩:AI浪潮的歷史拐點
- 有片/泰國警察也略懂!以舞獅為掩護逮捕慣竊
- 國際金價似站穩5000美元 分析看好年底衝上6500
- 日相高市第二任施政演說提中國「脅迫」 宣布新設國家情報委員會
- 遭判無期徒刑 尹錫悅道歉但堅稱戒嚴是為了「拯救國家」
- 「BTS」V私聊閔熙珍被當呈堂證供 強調沒選邊:感到錯愕
藍委質疑高端流感疫苗臨床試驗不全 食藥署:韓國數據能代表亞洲人
2023-10-18 11:09 / 作者 胡順惠

食藥署例行記者會說明高端流感疫苗臨床試驗。胡順惠攝
國民黨立委王鴻薇昨日提出質疑,高端流感疫苗臨床試驗僅針對20至50歲進行試驗,又以機密理由拒公開韓國GC公司的疫苗資料,如何讓人民相信?食藥署副署長陳惠芳今(10/18)日表示,高端有檢附韓國第一期到第三期臨床試驗,等於有亞洲人種資料,因此認為可支持其療效及安全性,無須在我國執行全年齡層臨床試驗。陳惠芳今日在例行記者會上說明,對於四價流感疫苗查驗登記,都一定要審核通過確保品質有效性才會核發許可證,臨床試驗並未限定試驗執行地點,而是視廠商所附整體臨床試驗數據結果進行審查其療效及安全性。
陳惠芳指出,依據ICH E5所訂的銜接性試驗基準審視該藥品是否具有族群差異,若經評估無族群差異者,得引用國外臨床試驗數據資料,未要求必須於我國執行臨床試驗或執行全年齡層臨床試驗,以減少重複進行臨床試驗。
陳惠芳舉例,像是跨國疫苗廠,以Covid-19疫情來說,因應疫情在不同國家原液做分裝充填,除非填充後跟原來不同,依照這樣的原則,所有疫苗案子審查都用同樣標準。
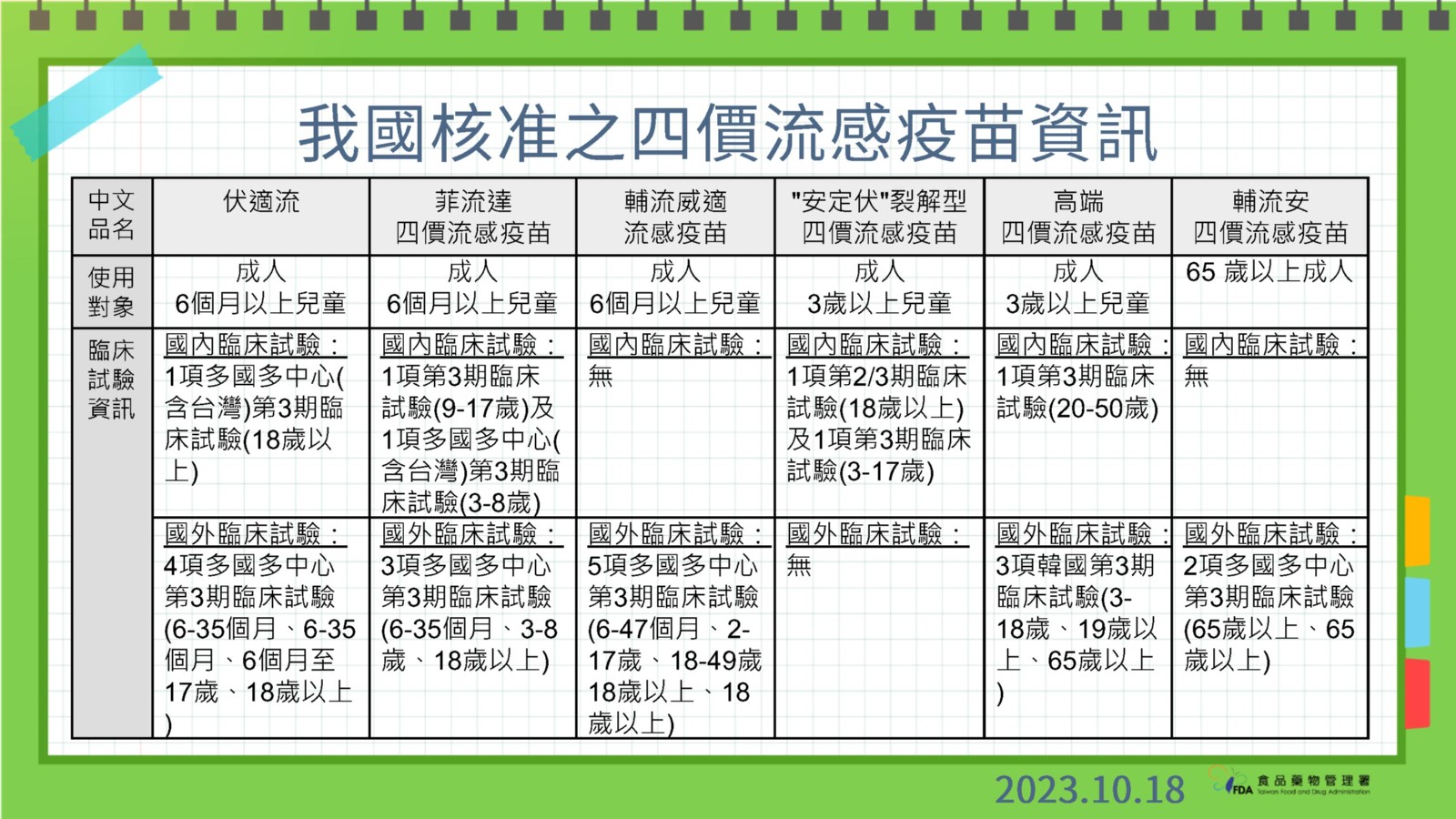
國內審核通過的6家流感疫苗資訊。食藥署提供
陳惠芳說,「高端四價流感疫苗」查驗登記案中,臨床試驗資料已檢附韓國執行的第一、第二期及第三期臨床試驗,受試者年齡包括3至18歲、19歲以上及65歲以上資料,也在我國執行第三期臨床試驗以受試者年齡:20至50歲。
因此,綜合韓國及台灣臨床試驗結果,陳惠芳指出,韓國等於有亞洲人種資料,沒有人種差異,國際上都是看人種差異,而非執行地點,因此認為可支持其療效及安全性,沒有要求全年齡層要在國內進行試驗。
至於為何不能提供臨床試驗資料?陳惠芳說依照藥事法第40-1條及營業秘密法第2條規定,藥品查驗登記時所檢附原始數據屬營業秘密資料,食藥署應保密,不過臨床試驗相關資料都有摘錄重點在仿單中,仿單可到許可證查詢系統查詢。
陳惠芳強調,所有核准的四價流感疫苗都是經由同樣標準審核,確認能達到有效性品質達一定規範才會放行,疫苗上市前一定要先檢驗、封緘才能放行供國人使用。
藥品組簡任技正黃玫甄也補充,國外數據完整情況下,可以直接引用國外數據申請許可證,只要有亞洲族群的數據就可以,不一定要做臨床試驗。
最新more>
- 北投泡溫泉兼吃美食 北投市場黑金滷肉飯、放山雞料理獲推薦
- 快訊/美國最高法院判決川普關稅違法 「法律未授權總統徵收關稅」
- 日外相國會演說再提「竹島主權」 南韓召見公使抗議
- 美國去年第4季經濟成長放緩 全年成長為近3年最差
- 廉航德威加入 南韓所有航空禁止機上使用行動電源
- 日本最年輕冬奧金牌選手背後的男人:為她做飯、開車接送「妹妹總有一天會站上世界舞台」
- 插隊搶自由座!高鐵白衣男爆出是牙醫 黑歷史曝光、退追柯文哲
- 江蕙唱一半見她衝上台突認有壓力 江淑娜搶穿戰袍討紅包
- 國道初四73起事故「回堵最長7公里」 明天北返車多!11條魔王路段曝光
- 前線照片打臉政府「沒埋地雷」說法 2柬埔寨記者遭叛國罪重判14年
熱門more>
- 分析:中國對非洲全境宣布零關稅政策 但想倚重的非洲同伴是哪種國家?
- 谷愛凌在美生長卻代表中國出賽 美副總統范斯說話了
- 「今天,我為龍一滑冰!」七年羈絆逆轉勝 「璃龍組」為日本雙人花滑摘首金
- 谷愛凌為何棄美投中?美媒:中國提供數百萬美元資金
- 2026最受矚目「漫改真人版」要來了!《我獨自升級》、《驀然回首》、《海洋奇緣》期待值爆表
- 日本雙人花滑「木原運送」超吸睛!木原龍一親揭原因:不希望璃來受傷
- 「森林鬼魅」寶寶露臉 蹦跳高手從6樓高躍下也沒事
- 同為華裔冬奧明星 為何谷愛凌被罵叛徒?劉美賢頂六四光環?
- 「週末都在工地搬磚」苦等12年冬奧終摘銀 他頒獎台上跪拜叩首
- 川普關稅擋不了逆差擴大 台灣貨品貿易逆差翻倍

